发布时间:2024-06-14 浏览次数:748
新版ISO 17511非常强调参考物质的互换性。水木济衡作为国产全品类第三方质控品综合服务商,一直以来也十分关注和重视法规、标准对产品的要求,我也曾发系列文章《对体外诊断试剂参考物质互换性的思考》,分享对互换性的学习和理解。
对体外诊断试剂参考物质互换性的思考
点击阅读原文
互换性概念的“前世今生”
(https://mp.weixin.qq.com/s/s9U6WfSa_BHSN5Dl_hDfbw)
Why Commutability Matters(互换性为什么很重要)
(https://mp.weixin.qq.com/s/eXVlWx4shydYXEj30sKq9g)
Commutability Still Matters(互换性仍然很重要)
(https://mp.weixin.qq.com/s/CctoatyuNmhiOOaYHtn6CA)
The evolving role of commutability inmetrological traceability(互换性在计量溯源性中的演进作用))
(https://mp.weixin.qq.com/s/ajKi7_bc4qabFS3n35kmGg)
去年W. Greg Miller、Neil Greenberg等学者在Clinical Chemistry发表了一篇专题报告,题目为《Guidance on Which Calibrators in a Metrologically Traceable Calibration Hierarchy Must Be Commutable with Clinical Samples(计量溯源校准层级结构上哪些校准品应与临床样品可互换)》。下面将文章的主要内容与大家做一个分享。

背景
VIM对互换性的定义是“互换性是参考物质的特性,由两个测量程序针对该参考物质的某一规定量进行测量所得结果之间关系,与针对其他指定物质的同一规定量进行测量所得结果之间关系的一致程度来表示”。在检验医学领域,“其他指定物质”是临床样品(CS),更通俗地讲,互换性可以理解为:参考物质的特性,参考物质对两个或更多的检测系统的响应,与临床样品对这些检测系统响应是相同的。校准品的基质与临床样品有差异,这样导致校准过程中引入了偏倚,在一定条件下可以通过增加一步纠正步骤予以消除这个偏倚。
ISO 17511:2020多处提到在给定的校准层级结构上各个步骤参考物质和校准品互换性的重要性,但是文件没有明确指出哪些校准品必须与CS是可互换的,哪些校准品的互换性不是必须的。如果一个校准品不具备互换性,但又被错误地使用,会造成接下来的测量发生偏倚,但同时评估互换性又是一个费时费力的事情,因此实施校准等级时,明确哪些校准品应具有互换性就显得尤为重要。这篇文章对ISO 17511:2020给出的溯源模型进行了进一步的明确:就某个溯源模型中,哪些校准品必须具备互换性?哪些校准品不做互换性要求?什么时候对应具备互换性而实际不具备互换性的校准品进行偏倚纠正?如何纠正?
何时要求校准品应具备互换性或可以不具备互换性
下表给出了ISO 17511:2020中校准层级结构中的各个要素,包括测量程序(p.1到p.6)和参考物质(m.1到m.6)。

ISO 17511:2020 的5.2章节给出了一个完整的溯源到SI单位的溯源模型,如下图Fig.1,A,被广泛接受的做法是,m.3是一组真实的临床样品(缩写为CS),将参考测量程序(p.3)的值传递到m.4,m.4去校准p.5(制造商常设测量程序),和(或)m.3将参考测量程序(p.3)的值直接传递到m.5,m.5去校准p.6(终端用户IVD-MD)。对于这一组真实的CS(m.3),只要制备、贮存的过程中没有改变,并且没有干扰性物质、不会对拟校准的测量程序p.4(制造商选定的测量程序)造成干扰,那么就认为这一组CS具备良好的互换性。用于校准p.5(制造商常设测量程序)的m.4(制造商工作校准品),通常由制造商来制备,应稳定,并能有足够的量用于后续很多年给m.5(终端用户IVD-MD校准品)赋值(制造商通常一年生产m.5多个批次,因此m.4的量要求要足够大)。大家都能理解,使用m.4校准p.5,而不是直接使用m.3校准p.5,这是因为m.3的稀缺性和珍贵性。
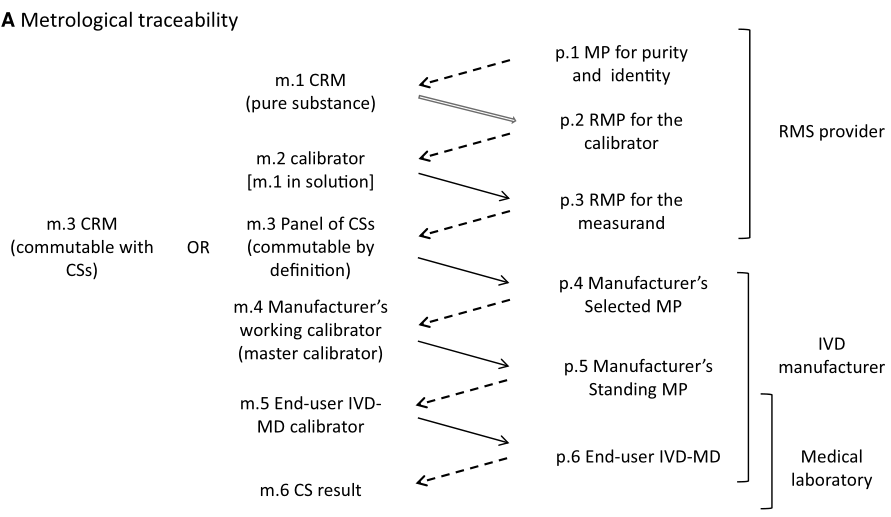
对于制造商而言,能有一个CRM(有证参考物质)作为m.3,比使用一组真实的临床样品作为m.3,在建立溯源性的时候更为经济,并且操作起来也更为简单可行。用作m.3的CRM应具备良好的互换性,能尽可能通用于所有市售的检测系统,从而便于制造商去建立实施他们产品的计量溯源。如果一个用作m.3的CRM对于大多数IVD产品具备互换性,只对一个或少数几个IVD产品不具备互换性,则有可能通过增加一个步骤来纠正因CRM不互换造成的偏倚。这个步骤可以在校准等级任何有意义的位置都可以进行,包括可以在p.6终端用户IVD-MD给出的校准模型或校准公式中。
当 P.4、P.5、P.6都是同一厂家生产的相同VD-MD
如下图所示。m.1是纯物质,对它没有互换性的要求。m.2是m.1配制的溶液,m.2校准p.3给m.3赋值,由于p.3一般是对m.2和m.3中的被测量具有高度选择性的参考测量程序(要符合ISO 15193的要求),并且也不受所测样品基质的影响,因此对m.2也不要求互换性。对于IVD厂家而言,使用与p.6(终端用户IVD-MD)相同的p.4(制造商选定的测量程序)、p.5(制造商常设测量程序)是厂家的常态和惯例,只不过p.4 和p.5更要严格操作和控制,并通过增加关键要素(校准品、测试样品、仪器)的重复测试(例如加大校准品的校准重复测试数、校准品分成多份、校准品使用多瓶、相同型号的仪器多使用几台)来减小给m.4和m.5赋值的不确定度。在这种情况下,m.3应在p.3和p.6之间具备互换性。如前所述,m.3当然可以直接校准p.6,但实际上没有这样操作的,这是考虑到m.3的稀缺性和珍贵性,所以才有了m.4和m.5作为量值传递的中间步骤。由于m.4和m.5只用于厂家自己的产品,因此没有必要要求m.4和m.5基质相同,也没有必要要求m.4、m.5要与临床样品(CS)基质相同,m.4和m.5可以是纯化学品溶于BSA或者其它缓冲液体系。
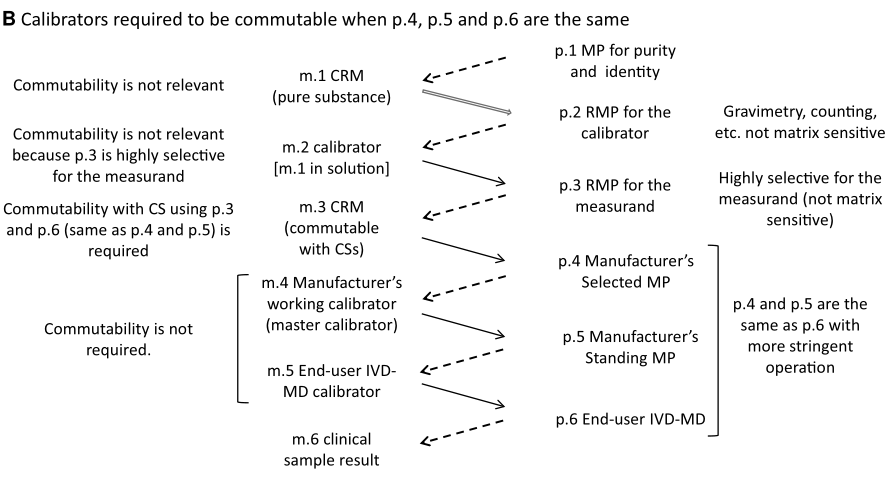
下面几张图来证明为何不对m.4和m.5作互换性要求,本文中这个过程是以校准曲线为直线的IVD试剂为例的,对于校准曲线为非直线的IVD试剂也能得到相同的结论。
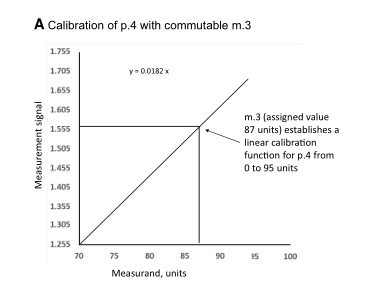
3.1下面A图中,m.3是具有互换性的CRM ,其浓度值是87 units,使用p.4测试出来的信号值是1.560,以0点和CRM这两点建立校准曲线。
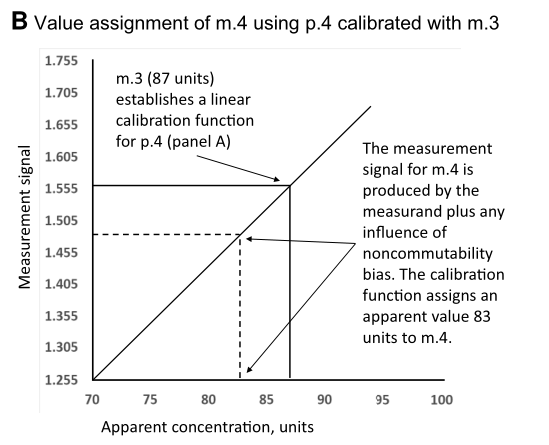
3.2下面B图中,m.4是制造商的master calibrator,使用p.4测试出来的信号值是1.483,这个信号值是受测量本身和m.4不互换带来的偏倚的综合影响而得出的,因此通过校准曲线得到的m.4浓度值83也反映了m.4不互换的影响。分配给m.4的值中任何不互换性偏倚大小都是不相关的,并且对不互换引起的偏倚纠正过来的被测量值的实际值也是不相关的。
3.3下面C图中,m.4的浓度是83,用p.5制造商常设测量程序测试得出的信号值是1.505。使用m.4和p.5做的校准曲线,其斜率(0.0179)与使用m.3和p.4做的校准曲线的斜率(0.0182)是不一样的,因为p.4和p.5是相同IVD-MD的不同实例。由于p.4和p.5是相同的IVD产品,因此它们受m.4不互换造成的影响程度是一样的。因此,p.5的校准曲线(当用m.4校准时)正确地反映了从可互换的m.3传递到m.4的测量值,并且p.5的线性校准曲线在计量学上可溯源到具有互换性的m.3。
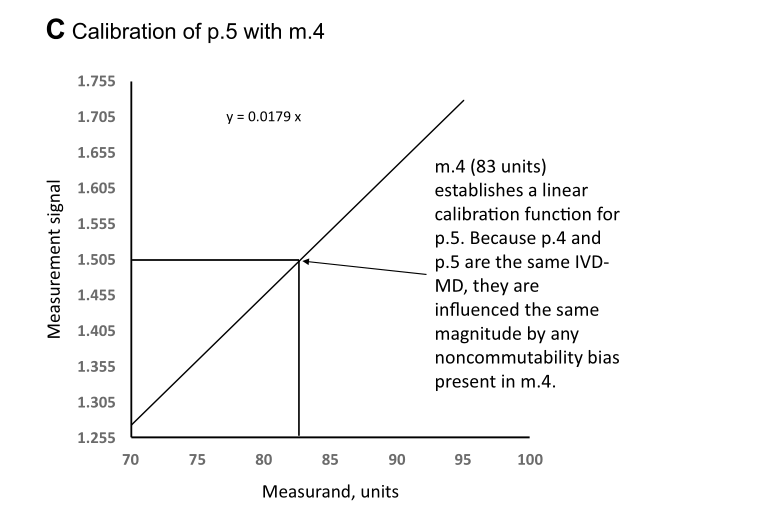
3.4下面D图中, 制造商终端用户产品校准品m.5 ,使用p.5测试得出的信号值是1.474,这个信号值是受测量本身和m.5不互换带来的偏倚的综合影响而得出的。使用m.4和p.5做的校准曲线,给m.5的赋值是81。因为p.4和p.5是相同的IVD-MD,它们在完全相同的程度上受到m.4或m.5中存在的任何不互换造成的偏倚的影响。m.5中任何不互换偏倚的大小都不相关,并且为不互换偏倚校正的被测量值的实际值也不相关。分配给m.5的值将补偿任何与基质相关的不互换偏倚,无论基质与m.4的基质相同还是不同。因为分配给m.4的值将值从可互换的m.3正确地转移到p.5的校准,所以p.5分配给m.5的值正确地补偿了m.5中可能存在的任何不互换偏倚的影响。
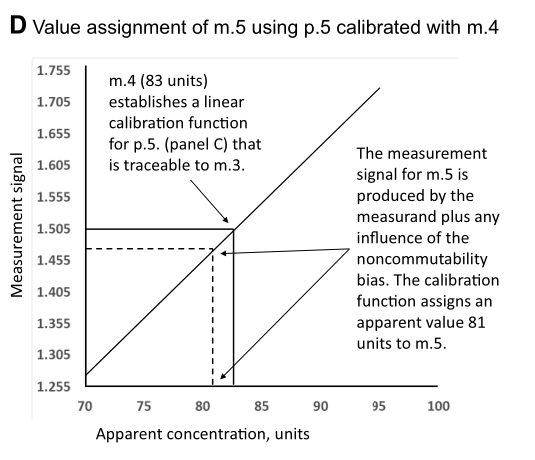
3.5下面E图中,m.5,其浓度赋值是81 units(使用m.4和p.5的校准曲线),使用p.6测出的信号值是1.464。p.6的校准曲线斜率(0.0181)与p.5的校准曲线斜率(0.0179)不同,因为这是同一个IVD-MD的不同实例。由于p.5和p.6是同一个IVD-MD,它们受到m.5存在的不互换引起的偏倚的影响,影响大小完全相同。因此,p.6的校准曲线正确地反映了从m.4转移到m.5的值,并依次正确地反映从m.3转移到m.4的被测量值。m.4或m.5中的任何不互换偏倚在其赋值中得到适当补偿,使得p.6最终用户IVD-MD的校准可直接溯源到m.3。
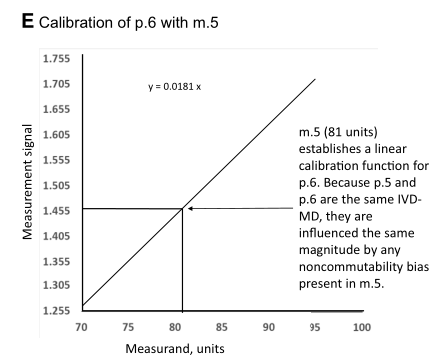
3.6下面F图中,m.6即临床待测样品(CS),使用p.6测试m.6得到其信号值1.410, 通过m.5和p.6建立起来的校准曲线给m.6的浓度是78 units。m.6的测量信号仅由m.6(CS)中的被测量产生,m.6是CS,不受互换性偏倚的影响。因此,分配给m.6(CS)的值可追溯到m.3中的被测量。m.4或m.5中可能存在的任何不互换偏倚,在给m.4或m.5赋值过程中得到补偿。最终临床样品的测量值是78 units。
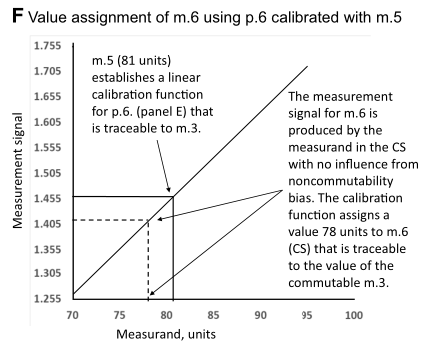
以上是一个全过程。注意,CS可能含有干扰物质,这些物质可能会影响测量信号,并由于p.6的选择性(以前称为特异性)不足而产生错误结果。测量程序的选择性与参考物质的互换性是不同的概念,但都会对量值传递产生影响。
m.4和m.5不需要与CS互换的一个基本条件是p.4、p.5和p.6都是来自同一制造商的同一个IVD-MD。如果这些MP中的一个不同,那么假设m.4或m.5的测量信号将受到任何与基质相关的不互换性偏倚的相同幅度的影响是不正确的,并且对所赋的值中的任何不互换偏倚的补偿将是无效的。
p.4与p.5、p.6不同的情况
同的情况,例如p.4是毛细管电泳法或液相色谱-质谱法,p.5、p.6可能是最终用户IVD-MD,例如使用分光光度法的试剂和仪器。m.1、m.2和m.3的互换性要求与前面第2章、第三章的描述相同。当m.3作为不同IVD-MD都可以通用的校准品时,要求m.3必须与m.6CS可互换。当p.4与p.5、p.6不同时,这种校准层次结构与上述的关键区别在于:m.4也必须在p.4与p.6之间与CS互换,这是因为p.4与p.6使用不同测量技术,因此对被测量具有不同的选择性,并受到与基质相关的不互换性偏倚的影响,并且影响程度还不一样。如果m.4在p.4和p.6之间互换,并且m.3在p.4和p.6之间也互换,则在使用p.4测试m.4的测量信号中不存在不互换引起的偏倚。m.4也可以是一组CS,假设它们不含有过量的干扰物质或其他样品特异性效应,则这样的m.4被认为是可互换的。
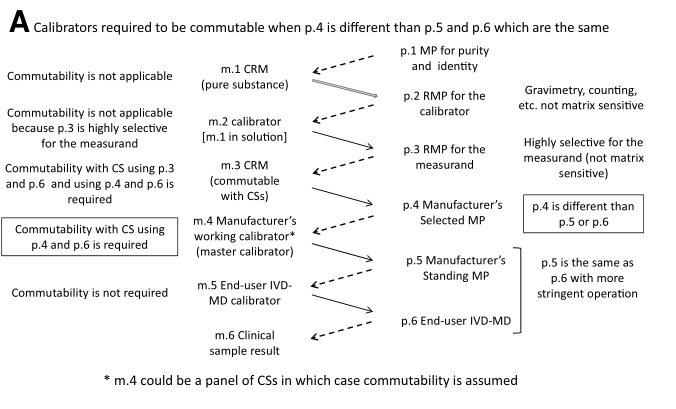
如果m.4不具有互换性,下图B显示在校准等级中,通过增加一步p.4a和m.4a如何将m.4中的不互换造成的偏倚进行纠正 ,具体步骤见这篇文献Miller WG, Budd J, Greenberg N, Weykamp C, Althaus H, Schimmel H, et al. IFCC working group recommendations for correction of bias caused by non-commutability of a certified reference material used in the calibration hierarchy of an end-user measurement procedure. Clin Chem 2020;66:769–78(这篇文献我将在下篇读书笔记中与大家分享)。
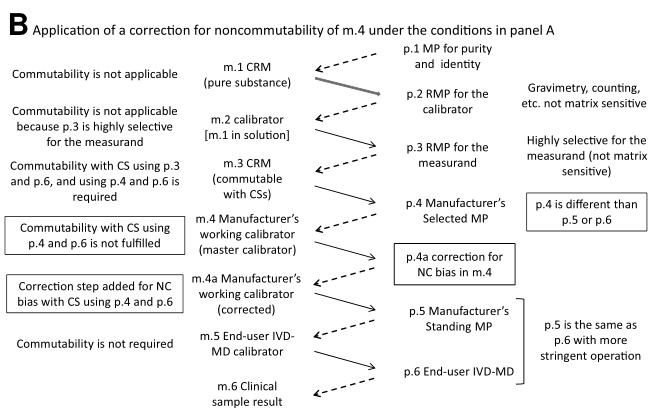
在p.4与p.5、p.6不同的情况下, m.5最终用户校准品不需要与m.6 CS互换,原因如前文所述,m.5中的任何不互换造成的偏倚都在给它的赋值中得到适当的补偿了。
没有高级别的纯品CRM或RMP的情况
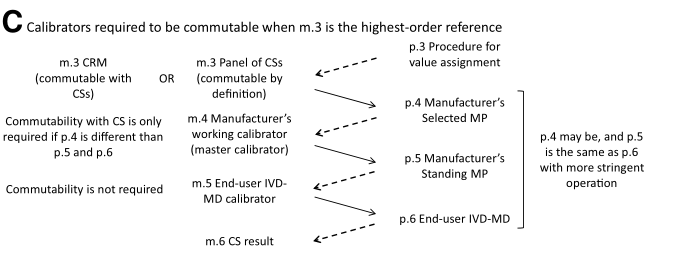
如下图C所示,没有高级别的纯品CRM,也没有符合ISO 15193的RMP,该校准层次结构正如ISO 17511:2020中的第5种模型所示。
在这种情况下,m.3是一组有临床样品(CS)组成的panel,通过一致化协议为其赋值。此种情况下,m.3 应具备互换性, 对m.4和m.5互换性要求同前文第2章、第3章所述。
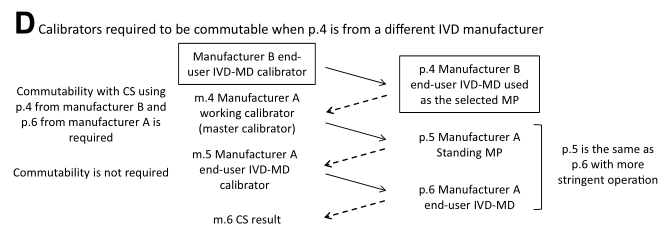
用另一个终端用户IVD-MD给工作校准品赋值的情况
如下图D所示,用另一个厂家的终端用户IVD-MD(B),作为选定的测量程序即p.4,来给A厂家的工作校准品赋值。在选择B产品时候,应优先考虑这些情况:B是用于制定医学决策标准的产品,或者对于该项目检测而言是“首台套”,或者是市场占有率最高的产品,或者被证明与已有的CRM最接近。在这种情况下,如果p.5和p.6都是A的同一个产品,A的工作校准品必须在p.6和用于给A 工作校准品赋值的B产品(即p.4)之间具备互换性。
m.4工作校准品是由RM添加到合适的基质制备而成的情况
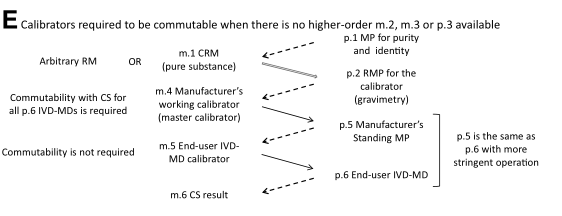
如下图E所示,在这种情况下,没有具备互换性的m.3,也没有p.3参考测量程序,相应地,m.2和p.4也就不适用了,这就是ISO17511:2020中第6种模型的变化形式。
当一个自定义的参考物质(尚到不了有证参考物质的等级)是m.4的原料时,计量溯源性的实施仅限于这一特定制造商的IVD-MD,对于同一被测量,这个IVD-MD与其他IVD-MD的校准层次没有明确的关系。
当具有纯度和浓度特征的纯物质CRM是m.4的原料时,应有一个能供所有制造商使用的较高等级的CRM。在该实施方案中,纯物质m.1在不同体外诊断MD之间实现与CS等效结果的有效性取决于所有厂家的m.4工作校准品是否与CS互换。每个制造商各自的m.4的互换性需要根据适当的协议来确定,不应预先假设它就有互换性。
在上面两种情况下,m.4都必须与CS互换,或者前文所述,对添加到校准层次中的不互换造成的偏倚进行校正。因为每个制造商都准备了自己的m.4,不同IVD-MD制造商可能会为m.4提供不同的基质。因此,互换性评估具有挑战性,对于单个IVD-MD制造商来说几乎是不可能的。在这种情况下,可以观察来自不同IVD MD的CS的结果等效性,原则上,可使用IFCC开发的校准有效性方法(见Budd JR, Weykamp C, Rej R, MacKenzie F, Ceriotti F, Greenberg N, et al. IFCC working group recommendations for assessing commutability part 3: using the calibration effectiveness of a reference material. Clin Chem 2018;64:465–74)进行互换性评估。
当使用国际一致化方案的情况
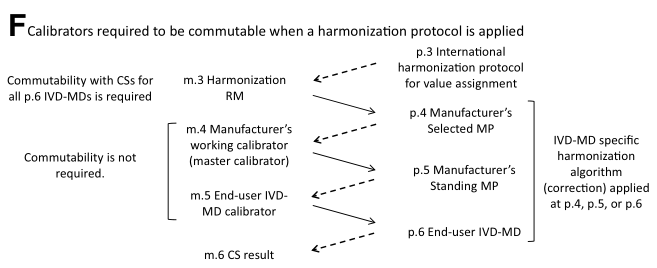
如下图F所示,如ISO 17511中的第5种模型和ISO 21151:2020中描述。在这种情况下,当使用所有制造商的p.6 终端用户IVD MD进行测量时,m.3(一致化RM)必须与CS可交换,因为其目的是为每个校准层次开发IVD-MD特定的校正算法,以实现使用任何IVD-MD测量CS的等效结果。一致化RM通常是一组未改变的CS。在一致化方案中,来自现有校准层次结构中任何来源的任何校准偏倚,包括IVD-MD制造商的m.4或m.5不互换引起的偏倚,都是通过在校准层级结构中开发和应用IVD-MD特定一致化算法来校正的。在实施一致化算法后,每个制造商都要采取必要的措施确保校准层次中的任何不互换偏倚保持不变。
使用m.4和m.5的限制
重要的是要认识到,一个体外诊断制造商的m.4和m.5不能与任何其他制造商的IVD-MD一起使用,因为这些校准品是为了满足一个特定IVD-MD的校准层次的技术要求而制造的。因此,对给m.4或m.5的赋值中的不互换引起的偏倚的任何补偿都是特定于一个制造商的p.5和p.6的。把一个IVD-MD制造商的m.4或m.5用到另一个制造商的IVD-MD可能会引入未知大小的偏倚,从而会对m.6产生错误的结果。
结论
识别校准层次结构中特定CRM或其他校准品何时需要与CS互换是成功实施IVD-MD计量溯源性的重要细节。对于哪些校准品必须与CS互换,没有一个简单的建议,因为根据高级别参考系统的可用性不同,可能有几种不同类型的校准层次。本报告为几种常见的计量溯源性情况提供了指导。
在具有互换性的RM不存在时,不互换引起的偏倚将传播到最终临床样品的测量结果。任何这种影响CS测量结果的不互换引起的偏倚都可以被量化,并且实施校正以调整过来。该校正的测量不确定度必须合并到CS的测量不确定度。
维持计量溯源性的前提是校准层次中所有元素的一致性和稳定性,尤其是校准品不互换引起偏倚时,任何变化,例如正在使用的校准品原材料供应商发生了变化,在实施变化前都必须仔细评估。
电话:010-69436691 / 13051159587
企业邮箱:smjh-sales@zgcsm.cn
公司地址:北京市北京经济技术开发区博兴五路10号1幢4层418、419
 微信公众号
微信公众号
 添加微信
添加微信
北京水木济衡生物技术有限公司 (C)2022-2026 京ICP备2021004626号-1