发布时间:2024-05-15 浏览次数:537
新版ISO 17511非常强调参考物质的互换性。水木济衡作为国产全品类第三方质控品综合服务商,一直以来也十分关注和重视法规、标准对产品的要求,我也曾发系列文章《对体外诊断试剂参考物质互换性的思考》,分享对互换性的学习和理解。
互换性概念的“前世今生”
(https://mp.weixin.qq.com/s/s9U6WfSa_BHSN5Dl_hDfbw)
Why Commutability Matters(互换性为什么很重要)
(https://mp.weixin.qq.com/s/eXVlWx4shydYXEj30sKq9g)
Commutability Still Matters(互换性仍然很重要)
(https://mp.weixin.qq.com/s/CctoatyuNmhiOOaYHtn6CA)
The evolving role of commutability
inmetrological traceability(互换性在计量溯源性中的演进作用))
(https://mp.weixin.qq.com/s/ajKi7_bc4qabFS3n35kmGg)
2019年意大利米兰大学的Federica Braga教授和Mauro Panteghini教授在Clin Chem Lab Med杂志发表了一篇Mini Review,题目为《Commutability of reference and control materials: an essential factor for assuring the quality of measurements in Laboratory Medicine(参考物质和质控物的互换性:保证检验医学测量质量的重要因素)》。下面将文章的主要内容与大家做一个分享。

溯源到一个通用的参照(理想情况下溯源到SI单位)能保证不同检测系统的测量结果的质量和等效。测量结果的溯源性通过一个不间断的校准链来实现,其中每项校准均会引入测量不确定度。
参考物质是“实验室标准化圣殿”的6大支柱之一(如下图所示,出自Braga F, Panteghini M. Verification of in vitro medical diagnostics (IVD) metrological traceability: responsibilities and strategies. Clin Chim Acta2014;432:55–61)。为了确保校准链的连续性,用于给制造商的校准品赋值的参考物质,其互换性应经过充分的调查和评价,“仅仅询问一种方法是否具有溯源性已经不够了; 溯源到一个具有互换性的参考物质,才具有真正的价值(it is no longer be enough to ask whether a method is traceable; traceability must be to a [reference] material demonstrated to be commutable to have true value) ”。

美国纽约州的公共卫生实验室沃兹沃斯中心生物化学实验室Robert Rej教授团队在进行临床酶活性检测中,发现一些商业质控品在不同方法学间的差异与病人血清不一样,因此于1973年首次提出“commutability”这一概念。尽管过去了50年,但大家对互换性的理解还是存在着混淆,对其研究也不多,文中对此做了一个统计。
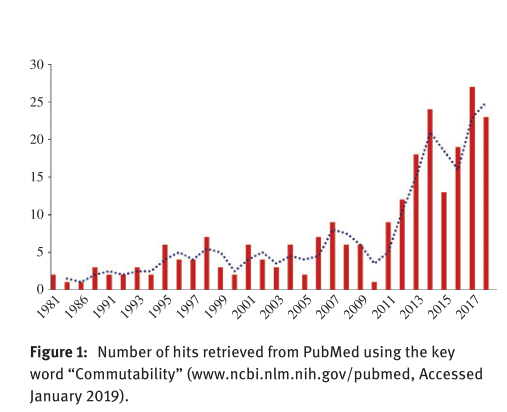
参考物质不具备互换性,其原因有两方面:
一是基质与临床样本有差别。
二是分析物与临床样本里的分析物有差别,下表做了一个分析。
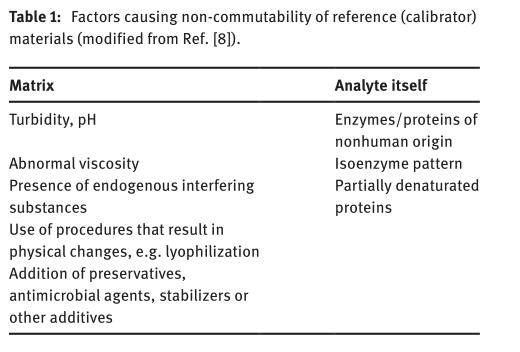
有研究发现使用电位法与比色法两种不同分析原理的方法进行锂的测量,IRMM的标准物质 BCR 304比NIST的标准物质SRM 956c表现出更好的互换性。
还有研究发现ERM-DA470k/IFCC中的白蛋白和免疫球蛋白A (IgA) 的互换性经过了确认,但是其中的铜蓝蛋白不具备互换性。
IFCC甲功检测标准化工作组的研究表明:使用不具备互换性的参考物质作为校准品,会造成溯源链的中断。该研究评价了16个TSH试剂盒,这些产品均声称溯源到WHO国际标准品94/674,但40份临床样品的检测结果有高达35%的变异,这么大的变异是因为94/674不互换造成的。
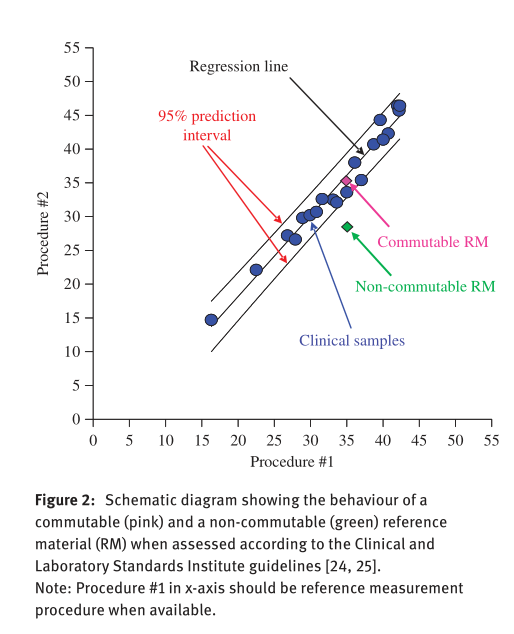
CLSI发布了两个互换性评价的标准:EP30-A和EP14-A3,其基本原理是选择20份天然的临床样本(CS),样本浓度能覆盖待评价的参考物质(RM),用一对程序(如参考测量程序和商品化试剂盒)检测RM和CS,进行回归分析,检查RM是否在由CS确定的95%的预定区间(PI)内,如下图所示。
这种方法有其局限性:
一是PI是统计学回归得出的,受比对的两个程序间的相关性影响,相关性越不好,却越容易得出RM具备互换性的结论;
二是以是否在PI内作为互换性可接受指标不能直接与RM的预期用途相关联;
三是受CS的影响(浓度、干扰因素等)。
2013年,IFCC成立了一个互换性工作组(WG-C),目标是改善RM互换性评价方法和标准。2018年,WG-C发布了三个文件:
——IFCC working group recommendations for assessing commutability Part 1:General experimental design
——IFCC working group recommendations for assessing commutability Part 2: Using the difference in bias between a reference material and clinical samples
——IFCC working group recommendations for assessing commutability Part 3: Using the calibration effectiveness of a reference material
Part 1提出互换性评价实验设计的关键成分,包括如何选择CS、检验程序的评价和纳入标准、互换性可接受的标准,并首次确定RM证书应给出的信息。
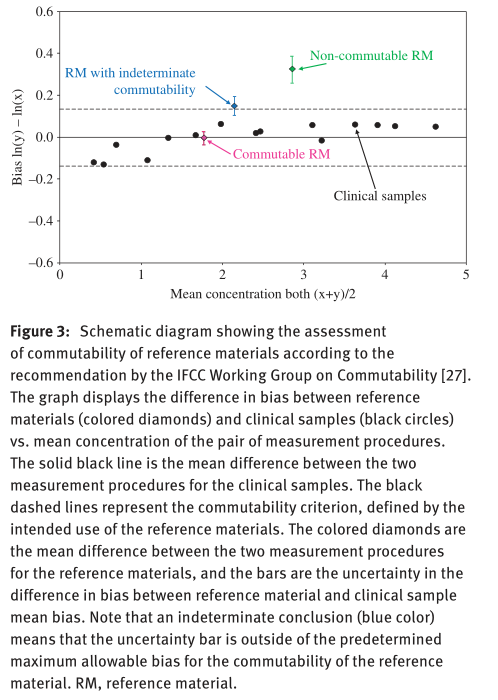
Part 2给出了一种互换性评价的方法,即验证RM在检测程序之间的系统差异与CS的平均偏倚之间的接近程度,如下图所示。
Part 3给出了另一个方法,基于这个RM用于校准不同检测系统后,对一致化的促进效果。候选RM被用于重新校准每个检测系统,如果它可以减少检测系统间的CV,则该RM视为可互换的。
相反,如果不能达到此效果,则该RM不具备互换性。IFCC的这两种方法都是以适合RM预期用途的预先设定的指标作为互换性可接受标准。
一般而言,用于溯源性链中的RM,应使用较严格的指标,对于质控物,指标可放宽一些。指标可采用2014年米兰EFLM会议中确定的模式。文中最后强调用于EQA的质控物,应保证其互换性。
电话:010-69436691 / 13051159587
企业邮箱:smjh-sales@zgcsm.cn
公司地址:北京市北京经济技术开发区博兴五路10号1幢4层418、419
 微信公众号
微信公众号
 添加微信
添加微信
北京水木济衡生物技术有限公司 (C)2022-2026 京ICP备2021004626号-1